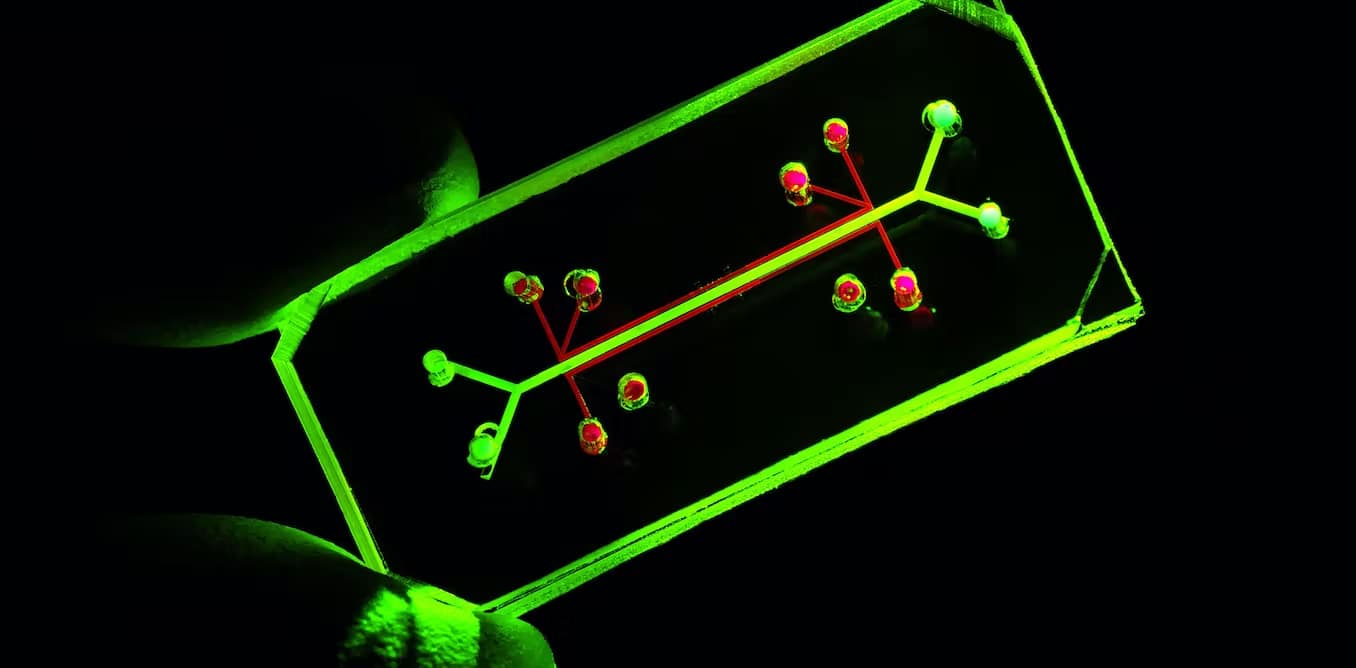
Ricostituire “organi su chip”, una via verso nuovi farmaci?
Portare un nuovo farmaco sul mercato costa miliardi di euro e può richiedere più di dieci anni. Questi enormi investimenti di tempo e denaro contribuiscono in modo determinante all’aumento vertiginoso dei costi sanitari e rappresentano ostacoli significativi per portare nuove terapie ai pazienti. Uno degli ostacoli risiede nei modelli di laboratorio utilizzati dagli scienziati per sviluppare farmaci.
Gli studi preclinici, ovvero gli studi che testano l’efficacia e la tossicità di un farmaco prima che entri negli studi clinici sull’uomo, vengono eseguiti principalmente su colture cellulari e animali. Questi due metodi sono limitati dalla loro scarsa capacità di riprodurre le condizioni del corpo umano. Le colture cellulari in una capsula di Petri non sono in grado di replicare tutti gli aspetti del funzionamento dei tessuti, come il modo in cui le cellule interagiscono nel corpo o le dinamiche degli organi viventi. E gli animali non sono umani: anche piccole differenze genetiche tra le specie possono essere amplificate in grandi differenze fisiologiche.
Meno dell’8% degli studi sugli animali riusciti per le terapie contro il cancro finisce negli studi clinici sull’uomo. Poiché i modelli animali spesso non riescono a prevedere gli effetti dei farmaci negli studi clinici sull’uomo, questi fallimenti tardivi possono aumentare significativamente i costi e i rischi per la salute dei pazienti.
Per risolvere questo problema di trasposizione, i ricercatori hanno sviluppato un modello promettente che può imitare più da vicino il corpo umano: l’organo su chip.
Cosa sono gli organi su un chip?
Alla fine degli anni ’90, i ricercatori hanno trovato un modo per stratificare polimeri elastici per controllare e analizzare i fluidi su scala microscopica. Nasce così il campo della microfluidica, che, nel campo delle scienze biomediche, prevede l’utilizzo di dispositivi in grado di mimare il flusso dinamico dei fluidi nel corpo, come il sangue.
I progressi nella microfluidica hanno fornito agli scienziati una piattaforma per far crescere cellule che funzionano come il corpo umano, specialmente con organi su un chip. Il “chip” si riferisce al dispositivo microfluidico che ospita le cellule. Di solito sono realizzati utilizzando la stessa tecnologia dei chip per computer.
Non solo gli organi su un chip imitano il flusso sanguigno nel corpo, ma queste piattaforme dispongono anche di microcamere che consentono di integrare più tipi di cellule per imitare i vari tipi di cellule normalmente presenti in un organo. Il flusso del fluido collega questi tipi di cellule, rendendo possibile studiare come interagiscono tra loro.
Questa tecnologia può superare i limiti delle colture cellulari statiche e degli studi sugli animali in diversi modi. In primo luogo, la presenza di fluidi circolanti nel modello gli consente di imitare sia ciò che una cellula sperimenta nel corpo, ad esempio il modo in cui riceve i nutrienti ed elimina i rifiuti, sia il modo in cui un farmaco viaggia attraverso il sangue e interagisce con diversi tipi di cellule. La capacità di controllare il flusso dei fluidi consente inoltre di mettere a punto il dosaggio ottimale di un particolare farmaco.
Il modello lung-on-a-chip, ad esempio, è in grado di incorporare le qualità meccaniche e fisiche di un polmone umano vivente. È in grado di imitare l’espansione e la contrazione, o inspirazione ed espirazione, del polmone e simulare l’interfaccia tra il polmone e l’aria. La capacità di riprodurre queste qualità permette di studiare meglio l’insufficienza polmonare in funzione di diversi fattori.
Come utilizzare maggiormente questa tecnologia?
Sebbene gli organi su un chip stiano spingendo i limiti della ricerca farmaceutica a monte, questa tecnologia non è stata ancora ampiamente integrata nelle pipeline di sviluppo dei farmaci. Si pensa che uno dei maggiori ostacoli all’ampia adozione di questi chip sia la loro elevata complessità e scarsa praticità.
Gli attuali modelli organ-on-a-chip sono difficili da usare. Inoltre, poiché la maggior parte dei modelli è monouso e consente un solo input, il che limita ciò che i ricercatori possono studiare in un dato momento, la loro implementazione è sia costosa che dispendiosa in termini di tempo e manodopera. Gli elevati investimenti necessari per utilizzare questi modelli potrebbero smorzare l’entusiasmo per la loro adozione. Dopo tutto, i ricercatori utilizzano spesso i modelli meno complessi disponibili per gli studi preclinici per ridurre tempi e costi.
È essenziale abbassare la soglia tecnica per la fabbricazione e l’utilizzo di organi su chip per consentire a tutta la comunità di beneficiare appieno dei loro vantaggi. Ma questo non significa necessariamente semplificare i modelli. Il laboratorio di Chengpeng Chen Professore di Chimica e Biochimica all’Università del Maryland, ad esempio, ha progettato diversi chip di tessuto pronti per l’uso, standardizzati e modulari, facilitando l’assemblaggio di parti prefabbricate per eseguire i loro esperimenti.
L’avvento della stampa 3D ha anche notevolmente facilitato lo sviluppo di organi su chip, consentendo ai ricercatori di fabbricare interi modelli di tessuti e organi direttamente su chip. La stampa 3D è ideale per la prototipazione rapida e la condivisione del design tra gli utenti e facilita anche la produzione di massa di materiali standardizzati.
Gli organi su un chip hanno il potenziale per consentire progressi nella scoperta di farmaci e una migliore comprensione di come funzionano gli organi, siano essi sani o malati. Rendendo questa tecnologia più accessibile, potremmo togliere il modello dallo sviluppo di laboratorio e lasciarlo prevalere nell’industria biomedica.
Autore
Chengpeng Chen, Università del Maryland, Contea di Baltimora